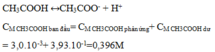Trong một dung dịch C H 3 C O O H , người ta xác định được nồng độ H+ bằng 3. 10 - 3 M và nồng độ C H 3 C O O H bằng 3,97. 10 - 1 M. Tính nồng độ mol ban đầu của C H 3 C O O H .

Những câu hỏi liên quan
Trong một dung dịch CH3COOH người ta xác định được nồng độ H+ bằng 3,0.10-3M và nồng độ CH3COOH bằng 3,93.10-1M. Nồng độ mol ban đầu của CH3COOH là: A. 0,390M B. 0,393M C. 0,396M D. 0,399M
Đọc tiếp
Trong một dung dịch CH3COOH người ta xác định được nồng độ H+ bằng 3,0.10-3M và nồng độ CH3COOH bằng 3,93.10-1M. Nồng độ mol ban đầu của CH3COOH là:
A. 0,390M
B. 0,393M
C. 0,396M
D. 0,399M
Mọi người giúp em làm bài tập các bài tập này nha. Bài nào cũng được ạ. Cảm ơn mọi người!
1. Hòa tan hết 26,5 gam NaCl trong 75 gam H2O ở 20°C được dung dịch X. Cho biết dung dịch X là bão hòa hay chưa bão hòa. Giải thích. Biết rằng độ tan của NaCl trong nước ở 20°C là 36 gam.
2. a) Hòa tan hết 7,18 gam NaCl vào 20 gam nước ở 20°C được dung dịch bão hòa. Xác định độ tan của NaCl ở nhiệt độ đó.
b) Xác định nồng độ phần trăm của dung dịch muối ăn bão hòa (ở 20°C), biết độ tan của NaCl ở nhiệt đ...
Đọc tiếp
Mọi người giúp em làm bài tập các bài tập này nha. Bài nào cũng được ạ. Cảm ơn mọi người!
1. Hòa tan hết 26,5 gam NaCl trong 75 gam H2O ở 20°C được dung dịch X. Cho biết dung dịch X là bão hòa hay chưa bão hòa. Giải thích. Biết rằng độ tan của NaCl trong nước ở 20°C là 36 gam.
2. a) Hòa tan hết 7,18 gam NaCl vào 20 gam nước ở 20°C được dung dịch bão hòa. Xác định độ tan của NaCl ở nhiệt độ đó.
b) Xác định nồng độ phần trăm của dung dịch muối ăn bão hòa (ở 20°C), biết độ tan của NaCl ở nhiệt độ đó là 36 gam.
3. Hòa tan hết 5,72 gam Na2CO3 . 10 H2O (sô đa tinh thể) vào 44,28 ml nước. Xác định nồng độ phần trăm của dung dịch thu được.
Cảm ơn mọi người
Trong dung dịch CH3COOH 4,3.
10
-
2
M, người ta xác định được nồng độ
H
+
bằng
8
,
6
.
10
-
4
mol/l. Hỏi có bao nhiêu phần trăm phân tử
C
H
3
C
O
O
H
trong dung dịc...
Đọc tiếp
Trong dung dịch CH3COOH 4,3. 10 - 2 M, người ta xác định được nồng độ H + bằng 8 , 6 . 10 - 4 mol/l. Hỏi có bao nhiêu phần trăm phân tử C H 3 C O O H trong dung dịch này điện li ra ion ?
Cho 10 gam một kim lọai X hóa trị II vào 200g H2O thì có 0,25 mol khí bay ra. Xác định kim lọai X. Tính nồng độ mol của dung dịch,nồng độ % dung dịch bazơ thu được.
Để xác định nồng độ của một dung dịch HCl, người ta đã tiến hành chuẩn độ bằng dung dịch NaOH 0,1 M. Để chuẩn độ 10 mL dung dịch HCl này cần 20 mL dung dịch NaOH. Xác định nồng độ của dung dịch HCl trên.
\(n_{NaOH}=0,02.0,1=0,002\left(mol\right)\\ HCl+NaOH\rightarrow NaCl+H_2O\\ \Rightarrow n_{HCl}=n_{NaOH}=0,002\left(mol\right)\\ \Rightarrow\left[HCl\right]=\dfrac{0,002}{0,01}=0,2M\)
Đúng 0
Bình luận (0)
ở 25 độ C nồng độ của dung dịch nacl bão hòa là 26 47 %
a .tính độ tan của nacl ở 25 độ C
b .người ta pha chế một dung dịch nacl ở 25 độ c bằng cách bão hòa 45 gam nacl vào 135 gam nước , hãy cho biết dung dịch nacl đã pha chế là đã bão hòa hay chưa . nếu dung dịch nacl là chưa bão hòa , hãy trình bày 2 cách làm khác nhau để có được dung dịch nacl bão hòa ở 25 độ C (bằng tính toán cụ thể)
Đọc tiếp
ở 25 độ C nồng độ của dung dịch nacl bão hòa là 26 47 %
a .tính độ tan của nacl ở 25 độ C
b .người ta pha chế một dung dịch nacl ở 25 độ c bằng cách bão hòa 45 gam nacl vào 135 gam nước , hãy cho biết dung dịch nacl đã pha chế là đã bão hòa hay chưa . nếu dung dịch nacl là chưa bão hòa , hãy trình bày 2 cách làm khác nhau để có được dung dịch nacl bão hòa ở 25 độ C (bằng tính toán cụ thể)
Ở 25 độ C , S = 36 (g)
\(\rightarrow\) Có 36 g NaCl tan trong 100g H2O tạo thành 136g ddbh
\(\rightarrow\) C%NaCl bão hòa = mctmdd.100%=36136.100%=26,47%
a) Người ta pha chế một dung dịch NaCl ở 20oC bằng cách hòa tan 23,5 gam NaCl trong 75 gam nước. Căn cứ vào độ tan của NaCl trong nước là 32 gam. Hãy cho biết dung dịch NaCl đã pha là bào hòa hay chưa bão hòa.
b) Ở nhiệt độ 25oC, độ tan của NaCl là 36 gam. Hãy tính nồng độ phần trăm của dung dịch bão hòa trên.
c) Có bn gam muối ăn trong 500 gam dung dịch bão hòa muối ăn ở 25oC. Biết độ tan ở nhiệt đợ này 36oC.
Đọc tiếp
a) Người ta pha chế một dung dịch NaCl ở 20oC bằng cách hòa tan 23,5 gam NaCl trong 75 gam nước. Căn cứ vào độ tan của NaCl trong nước là 32 gam. Hãy cho biết dung dịch NaCl đã pha là bào hòa hay chưa bão hòa.
b) Ở nhiệt độ 25oC, độ tan của NaCl là 36 gam. Hãy tính nồng độ phần trăm của dung dịch bão hòa trên.
c) Có bn gam muối ăn trong 500 gam dung dịch bão hòa muối ăn ở 25oC. Biết độ tan ở nhiệt đợ này 36oC.
Đốt cháy hoàn toàn 13,44 gam một muối sunfat của kim loại M hóa trị II , bằng lượng oxi vừa đủ thu được chất rắn A và khí B . Hòa tan A bằng dung dịch H2SO4 13,720% ( vừa đủ ) thu được dung dịch muối nồng độ 20,144% làm lạnh dung dịch này đến toC thấy tách ra được 12,50 gam tinh thể T , phần dung dịch bão hòa có nồng độ 14,589%
a) Xác định kim loại M và công thức của tinh thể T . Biết trong các phản ứng trên M có hóa trị không đổi
b) Tính độ tan của muối trong dung dịch bão hòa ở toC
Đọc tiếp
Đốt cháy hoàn toàn 13,44 gam một muối sunfat của kim loại M hóa trị II , bằng lượng oxi vừa đủ thu được chất rắn A và khí B . Hòa tan A bằng dung dịch H2SO4 13,720% ( vừa đủ ) thu được dung dịch muối nồng độ 20,144% làm lạnh dung dịch này đến toC thấy tách ra được 12,50 gam tinh thể T , phần dung dịch bão hòa có nồng độ 14,589%
a) Xác định kim loại M và công thức của tinh thể T . Biết trong các phản ứng trên M có hóa trị không đổi
b) Tính độ tan của muối trong dung dịch bão hòa ở toC
a) 2MS + 3O2 \(\rightarrow^{t^o}\) 2MO + 2SO2
x------------------------x--------x
\(\Rightarrow\) Chất rắn A là MO ; Khí B là SO2
MO + H2SO4 \(\rightarrow\) MSO4 + H2O
x-------x-----------x
Ta có : \(\dfrac{\left(M+96\right)x}{\left(M+16\right)x+\dfrac{98x}{13,72\%}}=20,144\%\)
\(\Rightarrow\) M = 64 ( Cu ) \(\Rightarrow x=\dfrac{13,44}{96}=0,14\left(mol\right)\)
\(\Rightarrow\) mdung dịch sau = 80 . 0,14 + \(\dfrac{98\cdot0,14}{13,72\%}=111,2\left(g\right)\)
\(\Rightarrow\)mdung dịch ( sau làm lạnh ) = 111,2 - 12,5 = 98,7 ( gam )
Gọi y là số mol CuSO4 còn lại trong dung dịch bão hòa . Ta có :
\(C\%_{CuSO_4}=\dfrac{160y\cdot100\%}{98,7}=14,589\%\Rightarrow y=0,09\left(mol\right)\)
\(\Rightarrow n_{CuSO_4.nH_2O}=n_{CuSO_4\left(táchra\right)}=0,14-0,09=0,05\left(mol\right)\)
\(\Rightarrow m_{CuSO_4.nH_2O}=0,05\cdot\left(160+18n\right)=12,5\left(g\right)\)
\(\Rightarrow n=5\left(CuSO_4.5H_2O\right)\)
b) Khối lượng nước trong dung dịch CuSO4 bão hòa :
\(m_{H_2O}=98,7-0,09\cdot160=84,3\left(g\right)\)
\(\Rightarrow S_{CuSO_4}=\dfrac{0,09\cdot160\cdot100}{84,3}=17,08\left(g\right)\)
Đúng 0
Bình luận (2)
Vì bài này dài nên mk chỉ làm tắt thôi nhé!
a) PTHH: 2MS + 3O2 --> 2MO + 2SO2
a a a
MO + H2SO4 --> MSO4 + H2O
a a a
Gọi a là số mol của MS
Ta có: \(\dfrac{m_{MSO_4}}{m_{MO}+m_{H_2SO_4}}\) = \(\dfrac{a\left(M+96\right)}{a\left(M+16\right)+\dfrac{98a}{13,72\%}}\) = 20,144%
=> \(\dfrac{M+96}{\dfrac{98}{13,72\%}+M+16}\) = 20,144%
Giải ra ta được: M = 64 (Cu) => \(a=\dfrac{13,44}{96}\) = 0,14 mol
=> \(m_{dd}\) sau p/ứ = \(m_{MO}+m_{dd.H_2SO_4}\) = \(\dfrac{98\times0,14}{13,72\%}+80\times0,14\) = 111,2 (g)
=> mdd sau khi làm lạnh = 111,2 - 12,5 = 98,7
PTHH: CuO + H2SO4 --> CuSO4 + H2O
Gọi b là số mol CuSO4 còn lại
Theo bài ra ta có:
C% CuSO4 = \(\dfrac{m_{ct}}{m_{dd}}\times100\%\) = \(\dfrac{160b}{98,7}\) \(\times\) 100% = 14,589%
=> b = 0,09 mol
=> nCuSO4 đã tách ra = 0,14 - 0,09 = 0,05 mol
=> \(n_{CuSO_4.xH_2O}\) =0,05 mol
=> 0,05 ( 160 + 18x ) = 12,5
=> x = 5
=> Tinh thể T là CuSO4.5H2O
b) Ta có: \(m_{H_2O}\) trong dd bão hòa = 98,7 - 0,09 x 160 = 84,3g
=> S của CuSO4 = \(\dfrac{160\times0,09\times100}{84,3}\) = 17,08g
Đúng 0
Bình luận (1)
Khi hòa tan một lượng của một oxit kim loại hóa trị II vào một lượng vừa đủ dung dịch axit H\(_2\)SO\(_4\) 4.9%, người ta thu được một dung dịch muối có nồng độ 5.78%. Xác định công thức của oxit trên.
Gọi kim loại đó là X
PTHH:\(XO+H_2SO_4\underrightarrow{ }XSO_4+H_2O\)
số mol của XO là a
\(m_{dd\left(H_2SO_4\right)}=\dfrac{98a}{4,9}.100\%=2000a\)
\(m_{dd}=XSO_4=\dfrac{a\left(X+96\right)}{5,78}.100\%\)
Mà \(m_{dd\left(XSO_4\right)}=m_{dd\left(H_2SO_4\right)}+m_{XO}\)
\(\Rightarrow\dfrac{a\left(X+96\right)}{5,78}.100=2000+a\left(X+16\right)\)
\(\Rightarrow\dfrac{\left(X+96\right)}{5,78}.100=2000+\left(X+16\right)\) rồi bạn giải ra giống pt
=>X=24 do đó X là Mg
PTHH:\(XO+H_2SO_4\underrightarrow{ }XSO_4+H_2O\)
số mol của XO là a
\(m_{dd\left(H_2SO_4\right)}=\dfrac{98a}{4,9}.100\%=2000a\)
\(m_{dd}=XSO_4=\dfrac{a\left(X+96\right)}{5,78}.100\%\)
Mà \(m_{dd\left(XSO_4\right)}=m_{dd\left(H_2SO_4\right)}+m_{XO}\)
\(\Rightarrow\dfrac{a\left(X+96\right)}{5,78}.100=2000+a\left(X+16\right)\)
\(\Rightarrow\dfrac{\left(X+96\right)}{5,78}.100=2000+\left(X+16\right)\) rồi bạn giải ra giống pt
=>X=24 do đó X là Mg
Đúng 0
Bình luận (0)